การทำโปรไฟล์เมตาโบโลมิกโดยใช้ LC-Q-Orbitrap HRMS
โดยทั่วไปการศึกษาเกี่ยวกับเมแทบอลิซึมเกี่ยวกับ ซัลเวีย สปีชีส์ในโหมดอิออไนเซชันเชิงลบมีแนวโน้มที่จะมีประสิทธิภาพมากกว่าสปีชีส์เหล่านี้ในโหมดบวก15- ในการศึกษานี้ การวิเคราะห์ข้อมูล MS รวมถึงการใช้ฐานข้อมูลออนไลน์และฐานข้อมูลท้องถิ่นที่จัดทำโดยซอฟต์แวร์ Compound Discoverer 2.1 นอกจากนี้ข้อมูลที่รวบรวมจากการศึกษาด้านเมตาบอลิซึมครั้งก่อนๆ ซัลเวีย สายพันธุ์ถูกรวบรวมและรวมเข้าเป็นรายการจำนวนมากเพื่อนำไปใช้เป็นฐานข้อมูลท้องถิ่น ตรวจพบพีคของสารทั้งหมด 2,704 พีค เอส. ฟรุติโคซา สกัดด้วยการวิเคราะห์โหมดไอออนลบ หลังจากกรองสัญญาณรองออกแล้ว (พื้นที่ < 104) มีสารเมตาบอไลต์ 98 ชนิด ซึ่งมีการระบุเบื้องต้น 95 ชนิดดังแสดงในตารางเสริม S1.
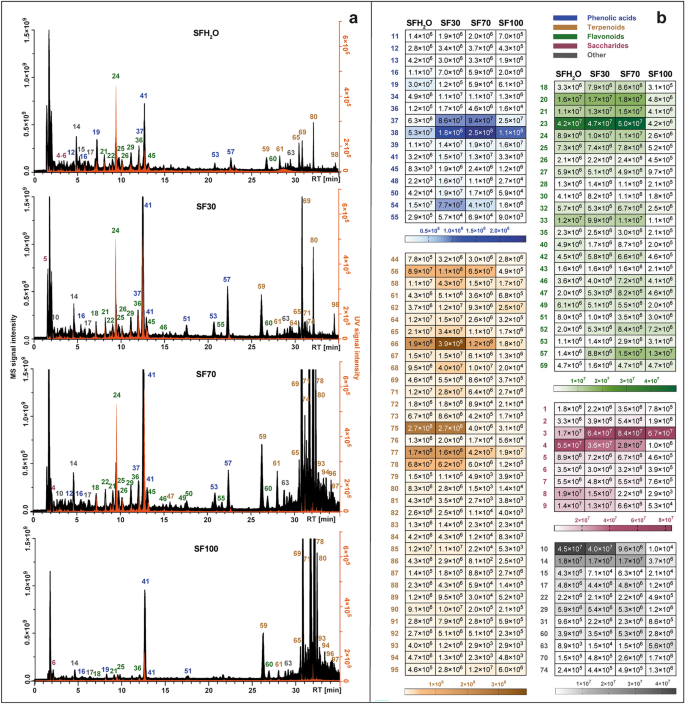
โปรไฟล์เมตาโบไลท์ของสารสกัดแต่ละชนิดถูกวางชิดกันและแสดงไว้ในรูปที่ 1ก. กลุ่มที่โดดเด่นมีการเปลี่ยนแปลงไปตามสารสกัดที่แตกต่างกัน ในตัวทำละลายที่มีน้ำเป็นส่วนใหญ่ (SFH2O และ SF30) สารประกอบที่มีมากที่สุดคือกรดฟีนอลิก ประสิทธิภาพการสกัดของสารประกอบเทอร์พีนอยด์สอดคล้องกับการเพิ่มขึ้นของเอธานอลในตัวทำละลายที่ใช้แล้ว เนื่องจากสารประกอบเหล่านี้มีลักษณะไม่มีขั้ว นอกจากนี้ แผนที่ความร้อนที่มีความเข้มของสัญญาณของไฟโตเคมิคอลแต่ละชนิดที่ตรวจพบใน 4 แบบที่แตกต่างกัน เอส. ฟรุติโคซา สารสกัดแสดงไว้ในรูป 1ข. สารประกอบประเภทจำนวนมากที่สุดที่ตรวจพบในสารสกัดที่ทำการศึกษาคือเทอร์พีนอยด์ที่มีสารประกอบ 35 ชนิด รองลงมาคือฟลาโวนอยด์ (สารประกอบ 24 ชนิด) กรดฟีนอลิกและอนุพันธ์ (19 สารประกอบ) แซ็กคาไรด์ (9 สารประกอบ) และอื่นๆ เช่น กรดไขมัน กรดคาร์บอกซิลิก และสารประกอบที่ไม่ระบุชื่อ .
โครมาโตกราฟีไอออนทั้งหมดที่ได้รับโดย LC-Q-Orbitrap ในโหมดเนกาทีฟ (สีดำ) รวมกับโครมาโตแกรมที่ลงทะเบียนโดยเครื่องตรวจจับ UV–Vis ที่ 270 นาโนเมตร (สีส้ม) (ก) ตั้งค่าด้วยแผนที่ความร้อนซึ่งแสดงถึงค่าพื้นที่พีคเฉลี่ยของ MS ของสารประกอบที่ระบุในสี่ค่าที่แตกต่างกัน เอส. ฟรุติโคซา สารสกัด : SFH2สารสกัด O-น้ำ; สารสกัดเอทานอล SF30–30%; สารสกัดเอธานอล SF70–70%; SF100–สารสกัดเอทานอล (ข- สำหรับเอกลักษณ์ของยอดเขา ดูตารางเสริม S1.
ในกรณีสารสกัดที่มีขั้วมากที่สุดถึง 2 ชนิด (SFH2O และ SF30) กรดฟีนอลิกเป็นคลาสที่มีมากที่สุดในพื้นที่พีคทั้งหมด คลาสนี้แสดงโดยอนุพันธ์ของกรดคาเฟอิกเป็นหลัก เวลาคงอยู่ (RT) ของสารประกอบ 16 โดยมีไอออนของสารตั้งต้น [MH]µ ที่ ม./ซ 179.03419 สอดคล้องกับ RT ของมาตรฐานกรดคาเฟอีน นอกจากนี้ยังสร้างลักษณะเฉพาะส่วนสำคัญที่ ม./ซ 135.04414 เนื่องจากการสูญเสียคาร์บอนไดออกไซด์ ตรวจพบกรดคาเฟอีนในรูปแบบ deprotonated ในสารประกอบ 40 และ 41ซึ่งถูกระบุว่าเป็นกรดซาเจอรินิก ([MH]′ ที่ ม./ซ 719.16210) และกรดโรสมารินิก ([MH]µ ที่ ม./ซ 359.0773) การระบุกรดโรสมารินิกได้รับการยืนยันเพิ่มเติมโดยการเปรียบเทียบกับมาตรฐาน มีการสังเกตไอออนเดียวกันหรือการสูญเสียของสารประกอบ 20, 37, 39, 44, 53, 57 และ 58ซึ่งสนับสนุนโดยการเปรียบเทียบกับวรรณกรรมและ MS2 การแยกส่วนถูกระบุว่าเป็นซัลเวียฟลาไซด์ ([MH] ′ ม./ซ 521.13012), กรดซัลเวียโนลิก B ([MH]µ ที่ ม./ซ 717.14661), กรดไอโซซัลเวียโนลิก B ([MH]′ ที่ ม./ซ 717.14667), กรดซัลเวียโนลิก K ([MH]′ ที่ ม./ซ 555.11469) ไอโซเมอร์ F ของกรดซัลเวียโนลิกสองตัว ([MH]µ ที่ ม./ซ 313.07205) และกรดซัลเวียโนลิก C ([MH]µ ที่ ม./ซ 491.09863).
ในกรณีของสารสกัดที่ไม่มีขั้วมากที่สุดสองชนิด (SF70, SF100) การมีส่วนร่วมของเทอร์พีนอยด์จะสูงที่สุด ในขณะที่สารสกัดที่เหลือในคลาสนี้คิดเป็นประมาณหนึ่งในสี่ของผลรวมของพื้นที่พีคของสารประกอบที่ระบุ คลาสนี้แสดงโดยไดเทอร์พีนอยด์เป็นหลัก ซึ่งเป็นสารประกอบไม่มีขั้วที่หลากหลายที่สุดที่ระบุในสารสกัดที่ศึกษา พวกมันส่วนใหญ่เป็นไดเทอร์พีนอยด์ประเภทอะบีเทน ซึ่งการแตกตัวผ่านการไอออไนเซชันเชิงลบมักรวมถึงการเอา CO ออก2 (-44 ดา), CO (-28 ดา), H2O (-18 ดา), ·CH3 (15 ดา). สารประกอบ 59 ([MH]Âที่ ม./ซ 345.17075) และ 64 ([MH]Âที่ ม./ซ 345.17100) ทั้งสองแสดงไอออนที่เกิดจากการสูญเสียโมเลกุลคาร์บอนไดออกไซด์ (ม./ซ 301.18097) และโมเลกุลของน้ำ (ม./ซ 283.17038 และ ม./ซ 283.17041) และถูกระบุเป็นโรสมานอลและเอพิไอโซรอสมานอล สารประกอบ 69 ([MH]Âที่ ม./ซ 329.17580) ถูกระบุว่าเป็นคาร์โนซอลตามรูปแบบการกระจายตัวโดยทั่วไป โดยเริ่มจากการสูญเสียคาร์บอนไดออกไซด์ (ม./ซ 285.16604)12,15 และตามด้วยการกำจัดอนุมูลเมทิล (ม./ซ 270.16211) รูปแบบการกระจายตัวเดียวกันเกิดขึ้นในสารประกอบ 80, ระบุว่าเป็นกรดคาร์โนซิก 12 เมทอกซี ([MH]′ที่ ม./ซ 345.20721) โดยมีแฟรกเมนต์ 301.21689 และ 286.19385 สารประกอบ 78โดยมีไอออนโมเลกุลเทียมอยู่ที่ ม./ซ 331.19153 [MH]′ ถูกระบุว่าเป็นกรดคาร์โนซิกเนื่องจากมีชิ้นส่วนที่เกี่ยวข้องกับการสูญเสียคาร์บอนไดออกไซด์และการสูญเสียอนุมูลไอโซโพรพิลในเวลาต่อมา (ม./ซ 287.20175 และ 244.14687) สารประกอบ 70 แสดงไอออนของสารตั้งต้นที่ [MH]µ ที่ ม./ซ 343.15524 ซึ่งสร้างชิ้นส่วนที่มีลักษณะเฉพาะ ม./ซ 315.16028 และ ม./ซ 299.160504 โดยการสูญเสียเอทิลีนและคาร์บอนไดออกไซด์ ตามลำดับ นั่นทำให้เราสามารถระบุสารประกอบได้ 70 เป็นโรสมาเดียล นอกจากนี้ ตรวจพบเพนตะไซคลิก ไตรเทอร์พีนอยด์ 2 ชนิดในสารสกัดที่ทดสอบ: สารประกอบ 96 และ 97ซึ่งได้รับการระบุเบื้องต้นว่าเป็นกรดเบทูลินิกและกรดเออร์โซลิก ตามลำดับ โดยมีไอออนควอซิโมเลกุลที่ ([MH]µ ที่ ม./ซ 455.35340) มีรายงานการมีอยู่ของสารไตรเทอร์พีนอยด์เหล่านี้ด้วย เอส. ฟรุติโคซา โดย Jash และคณะ16.
ในสารสกัดที่ศึกษาโดยเฉพาะสารสกัดที่มีปริมาณน้ำสูง (SFH2O, SF30) ส่วนแบ่งที่มีนัยสำคัญของโอลิโกแซ็กคาไรด์และกรดน้ำตาลในพื้นที่พีคทั้งหมดของสารประกอบที่ระบุยังถูกบันทึกไว้อีกด้วย สารประกอบ 1, 2 และ 3 ถูกระบุเบื้องต้นว่าเป็นสตาคิโอส ราฟฟิโนส และซูโครส เนื่องจากพวกมันมักเป็นน้ำตาลขนส่งหลักใน ซัลเวีย สายพันธุ์31- สารประกอบ 4–8 ถูกจัดเป็นกรดน้ำตาล รูปแบบการกระจายตัวของสารประกอบ 6 ([MH]Âที่ ม./ซ 135.02875) เหมือนกับของ ล-กรดทรีโอนิก สารประกอบ 8 ([MH]Âที่ ม./ซ 149.0081) สร้างแฟรกเมนต์ ม./ซ 72.99171, 59.01249 และ 87.00734 ที่สามารถสังเกตได้ในโหมดไอออนลบสำหรับ ล-( +)-กรดทาร์ทาริก
สารพฤกษเคมีที่สำคัญอีกประเภทหนึ่งที่ตรวจพบใน เอส. ฟรุติโคซา สารสกัดคือฟลาโวนอยด์ สารประกอบที่ระบุส่วนใหญ่อยู่ในกลุ่มนี้ถูกกำหนดให้เป็นฟลาโวน สารประกอบ 24 ได้รับการระบุอย่างชัดเจนว่าเป็นสคิวเทลลารินโดยการเปรียบเทียบเวลาการเก็บรักษา สเปกตรัม UV และรูปแบบการกระจายตัวของ MS/MS กับของมาตรฐานเชิงพาณิชย์ สารประกอบ 46 และ 55 แสดงไอออนของสารตั้งต้นที่เกือบจะเหมือนกัน [MH]′ ที่ ม./ซ 299.0563 และ 299.0562 สารประกอบ 46 ทำให้เกิดเศษชิ้นส่วนมากที่สุดที่ ม./ซ 284.03253 และ 136.98682 สารประกอบในทำนองเดียวกัน 55- ข้อมูลเหล่านี้สอดคล้องกับรูปแบบการกระจายตัวของฮิสพิดูลินหรือไดออสเมติน เนื่องจากมีความแตกต่างในเวลากักเก็บ สารประกอบทั้งสองจึงสามารถมีอยู่ได้ เอส. ฟรุติโคซา สารสกัด สารประกอบ 49 แสดงไอออนของสารตั้งต้นที่ [MH]µ ที่ ม./ซ 285.04065 ที่ก่อให้เกิดผลิตภัณฑ์ไอออนจำเพาะที่ ม./ซ 133.02834, 151.00261, 175.03903 ซึ่งสอดคล้องกับรายงานเกี่ยวกับลูทีโอลินโดย Velamuri และคณะ17- สารประกอบ 52 ([MH]Âที่ ม./ซ 327.21786) ถูกระบุว่าเป็น salvigenin (pectolinarigenin-7-methyl ether) เนื่องจากมีการรายงานฟลาโวนนี้ก่อนหน้านี้ใน เอส. ฟรุติโคซา- สารประกอบ 54 ให้ค่าพีคฐาน [MH]′ ที่ ม./ซ 269.04578. ไอออนตั้งต้นและไอออนผลิตภัณฑ์ ม./ซ 117.03332 และ 151.00264 ยืนยันว่าสารประกอบนี้คือเอพิเจนิน สารประกอบ 56 ให้ไอออนของสารตั้งต้น [MH]µ ที่ ม./ซ 329.0668 ซึ่งบ่งชี้ว่าสูตรโมเลกุลของมันคือ C17ชม14โอ7- มันผลิตไอออนชิ้นส่วนที่โดดเด่นที่ ม./ซ 299.01981 เนื่องมาจากการสูญเสียหมู่เมทิลสองหมู่ และ 271.02472 เนื่องมาจากการกำจัดคาร์บอนมอนอกไซด์เพิ่มเติม ดังนั้นจุดสูงสุดนี้จึงถูกระบุเป็นจาซีโอซิดิน สารประกอบ 60 ถูกระบุว่าเป็นซิซิมาริตินโดยอาศัยไอออนของสารตั้งต้น [MH] ′ที่ ม./ซ 313.07190 และไอออนผลิตภัณฑ์วินิจฉัยที่ ม./ซ 298.04694 และ 283.02478 บ่งชี้การสูญเสียอนุมูลเมทิลสองตัวและ 255.02974 จากการกำจัดคาร์บอนมอนอกไซด์ สารประกอบ 62 ([MH]Âที่ ม./ซ 283.06137) สอดคล้องกับอนุพันธ์ของเอพิเจนินเมื่อพิจารณาถึงชิ้นส่วนที่ ม./ซ 268.03772 และ 117.03318 ลักษณะเฉพาะของแฟรกเมนต์ไอออนที่ ม./ซ 240.04193 เกิดจากการสูญเสียคาร์บอนมอนอกไซด์ทำให้เกิดสารประกอบ 62 ถูกระบุว่าเป็นเก็นควานิน รูปแบบการกระจายตัวของ apigenin, hispidulin, cirsimaritin และ genkwanin นั้นสอดคล้องกับที่รายงานโดย Koutsoulas และคณะ12- สารประกอบ 50 เป็นฟลาโวนอลอะไกลคอนชนิดเดียวที่ตรวจพบในสารสกัดที่ศึกษา ด้วยสารตั้งต้นไอออน [MH]′ที่ ม./ซ 315.0513 และแฟรกเมนต์ MS/MS หลักที่ ม./ซ 300.02756 ซึ่งเป็นผลมาจากการสูญเสียหมู่เมทิล สารประกอบนี้ถูกระบุว่าเป็นไอโซแฮมเนติน สารประกอบ 30 โดยมีไอออนโมเลกุลเทียม [MH]′ ที่ ม./ซ 609.18329 ไม่ได้แสดงการกระจายตัวใดๆ แต่เนื่องจากมีการรายงานก่อนหน้านี้ เอส. ฟรุติโคซา18,19มันถูกระบุเบื้องต้นว่าเป็นฟลาโวโนน—เฮสเพอริดิน ฟลาโวนอยด์ไกลโคไซด์ที่พบในการศึกษานี้ส่วนใหญ่เป็นกลูโคไซด์โดยมีลักษณะเฉพาะคือ 162 Da, กลูคูโรไนด์ (176 Da) และรูติโนไซด์ (308 Da) ลูทีโอลิน กลูโคไซด์ (สารประกอบ 22 กับ [MH]Â ที่ ม./ซ 447.09344) มีอยู่ในสิ่งพิมพ์ส่วนใหญ่ที่เกี่ยวข้องกับองค์ประกอบทางเคมีของ เอส. ฟรุติโคซา สารสกัด12,18,19,20,21- สารประกอบ 26 แสดงไอออนของสารตั้งต้น [MH]′ ที่ ม./ซ 491.0836 และถูกระบุว่าเป็น isorhamnetin glucuronide ตามรายงานก่อนหน้านี้ เอส. ฟรุติโคซา โดยGürbüzและคณะเท่านั้น22- สารประกอบ 27 ([MH]Âที่ ม./ซ 577.15668) ซึ่งระบุว่าเป็น apigenin-rutinoside ยังพบในปราชญ์กรีกโดย Cvetkovikj และคณะ21.
นอกจากนี้ยังพบกรดไขมันใน เอส. ฟรุติโคซา สารสกัด สารประกอบ 63 และ 73 ถูกระบุเบื้องต้นว่าเป็นกรดไขมันไม่อิ่มตัวเชิงซ้อนสองตัว สารประกอบ 63 ถูกกำหนดให้เป็นกรดไดไฮดรอกซีออคตาเดคาไดอีโนอิก (C18ชม31โอ4). สารประกอบ 73 ทำให้เกิดสารตั้งต้นไอออน [MH]µ ที่ ม./ซ 295.22803 และชิ้นส่วนลักษณะเฉพาะที่ ม/z 277.21738 ([MHH2โอ]− และ 195.13837 [M-(CHO-(CH2)4-ช3)-H]′ ซึ่งระบุตำแหน่งของหมู่ไฮดรอกซิลที่อะตอมคาร์บอน 13 อะตอม ดังนั้นจึงถูกระบุว่าเป็นกรด 13-ไฮดรอกซี-9,11-ออคตาเดกาดีโนอิก นอกจากนี้ใน เอส. ฟรุติโคซา สกัดการมีอยู่ของกลูโคไซด์ของกรดทูเบอร์โรนิก (ม./ซ 387.16644) (สารประกอบ 14) ซึ่งเป็นฮอร์โมนการเจริญเติบโตที่ถูกสังเกต
การวิเคราะห์เชิงปริมาณของไฟโตเคมิคอลที่สำคัญ
ปริมาณสารประกอบฟีนอลหลักในสารสกัดต่างๆ เอส. ฟรุติโคซา ของน้ำหนักแห้งของวัสดุพืช (มก./กรัม DW) แสดงไว้ในตารางที่ 1 1- ปริมาณของกรดคาเฟอิก สคูเทลลาริน กรดซัลเวียโนลิก B กรดโรสมารินิก กรดคาร์โนซิก และคาร์โนซอล คำนวณโดยใช้เส้นโค้งการสอบเทียบของมาตรฐานที่แท้จริง ในขณะที่ปริมาณของสารประกอบอื่นๆ ได้รับการประเมินโดยสัมพันธ์กับมาตรฐานที่คล้ายกันที่สุดที่มีอยู่
โดยรวมแล้ว สารประกอบที่มีมากที่สุดในสารสกัดจากเสจคือกรดโรสมารินิก ซึ่งเป็นกรดฟีนอลิกและกรดคาเฟอิกเล็กน้อย ความเข้มข้นของกรดโรสมารินิกสูงสุดในบรรดาตัวอย่างที่ทดสอบทั้งหมดพบใน SF70 (31.56 ± 1.88 มก./กรัม DW) ซึ่งเหมือนกับความเข้มข้นของกรดโรสมารินิกใน เอส. ฟรุติโคซา เก็บจากโครเอเชีย (29.10 ± 0.21 มก./กรัม DW) รายงานโดย Mervić และคณะ23- มีรายงานปริมาณที่สูงกว่า (60.73 มก./กรัม DW) ในสารสกัดเมทานอลจากปราชญ์พันธุ์กรีกที่ศึกษาโดย Sarrou และคณะ19แต่ในการศึกษานี้ การใช้แอลกอฮอล์บริสุทธิ์เป็นตัวทำละลายไม่ได้ส่งผลให้ได้กรดโรสมารินิกสูงสุด ความเข้มข้นของกรด Rosmarinic ในการแช่ (SFH2O) ต่ำกว่าสารสกัดอื่นๆ มาก (4.96 ± 0.65 มก./กรัม DW) ซึ่งไม่สอดคล้องกับผลการเปรียบเทียบที่คล้ายกันสำหรับพันธุ์ตุรกี เอส. ฟรุติโคซา โดย เตคิน18- นอกจากนี้ ตรวจพบกรดคาเฟอีนในสารสกัดที่ศึกษาทั้งหมดที่ความเข้มข้นใกล้เคียงกัน (0.13–0.15 มก./กรัม DW) ซึ่งต่ำกว่าที่รายงานโดย Mervić และคณะ ถึงสิบเท่า23- อย่างไรก็ตาม มีกรดซัลเวียโนลิกเพียงไม่กี่ชนิดซึ่งเป็นของสารตัดแต่งกรดคาเฟอิกหลักในพืชเสจ มีอยู่ในปริมาณที่มากกว่า ความเข้มข้นสูงสุดของกรดซัลเวียโนลิก B ได้มาจากสารสกัด SF70 และ SF30 (6.86 ± 0.93 มก./กรัม DW และ 6.52 ± 0.48 มก./กรัม DW) กรดซัลเวียโนลิก K มีมากที่สุดในสารสกัด ST30 โดยมีความเข้มข้น 6.25 ± 1.0 มก./กรัม DW ตามข้อมูลที่นำเสนอโดย Cvetkovikj และคณะ21ความเข้มข้นสูงสุดของกรดซัลเวียโนลิก K ในกลุ่มประชากรชาวกรีกที่ศึกษาหลายกลุ่ม เอส. ฟรุติโคซา เท่ากับ 7.20 มก./กรัม DW
สารประกอบเทอร์พีนอยด์ที่มีมากที่สุดใน เอส. ฟรุติโคซา คือกรดคาร์โนซิกและคาร์โนซอล ซึ่งทั้งสองอยู่ในตระกูลของอะบีเทน ไดเทอร์พีนอยด์12- ปริมาณกรดคาร์โนซิกสูงสุดพบได้ใน SF100 (14.82 ± 1.66 มก./กรัม DW) ตามด้วย SF70 (13.88 ± 2.52 มก./กรัม DW) ซึ่งไม่แตกต่างกันทางสถิติ ผลลัพธ์เหล่านี้สอดคล้องกับเนื้อหาที่วัดได้ในสารสกัดเมทานอลโดย Kallimanis และคณะ24 ซึ่งก็คือ 12.5 ± 1.6 มก./ก. DW ปริมาณคาร์โนซอลในสารสกัด SF70 อยู่ที่ 7.88 ± 1.33 มก./ก. DW และสอดคล้องกับรายงานนี้โดย Sarrou และคณะ19- Salviol ซึ่งเป็นเทอร์พีนอยด์ที่มีมากเป็นอันดับสามในสารสกัดที่ศึกษา คือ meroterpenoid ที่ได้มาจาก abietane diterpenoid—ferruginol และพบได้ทั่วไปในปราชญ์สายพันธุ์กรีกอื่น ๆ เช่น ส.ปอมมิเฟรา25- สารประกอบนี้ยังไม่ได้รับการรายงานใน เอส. ฟรุติโคซา- อย่างไรก็ตาม มีอยู่ในสารสกัดที่ศึกษาส่วนใหญ่ที่มีปริมาณสูงสุด: 7.37 ± 0.71 มก./ก. DW ใน SF70
สารออกฤทธิ์ทางชีวภาพกลุ่มที่สามที่ตรวจพบใน เอส. ฟรุติโคซา สารสกัดเป็นฟลาโวนอยด์ Scutellarin เป็นหนึ่งในสารฟลาโวนอยด์ทั่วไปที่พบในปราชญ์26- เป็นฟลาโวนอยด์ที่มีมากที่สุดในสารสกัดที่ทำการศึกษาโดยให้ผลผลิตใกล้เคียงกัน: 7.77 ± 0.48 มก./กรัม DW, 8.92 ± 1.56 มก./กรัม DW และ 7.35 ± 0.9 มก./กรัม DW ใน SFH2สารสกัด O, SF30 และ SF70 ตามลำดับ ความเข้มข้นของลูทีโอลิน รูติโนไซด์และลูทีโอลินกลูโคไซด์มีความคล้ายคลึงกันในสารสกัดที่ศึกษาทั้งหมด และอยู่ระหว่าง 1.03 ถึง 1.98 มก./กรัม DW ซึ่งไม่สอดคล้องกับข้อมูลที่รายงานโดย Tekin และคณะ18โดยที่ความเข้มข้นของสารประกอบเหล่านี้ในการชงเสจนั้นสูงกว่าสารสกัดเอทานอลสองถึงสามเท่า
กรดฟีนอลิก ฟลาโวนอยด์ และเทอร์พีนอยด์เป็นสารประกอบออกฤทธิ์ทางชีวภาพทั่วไปใน เอส. ฟรุติโคซา- ดังแสดงในตาราง 1ผลผลิตการสกัดได้รับผลกระทบอย่างมากจากปริมาณเอทานอลในตัวทำละลาย การสกัดด้วยเอทานอล 70% ให้ผลผลิตรวมของสารออกฤทธิ์ทางชีวภาพสูงสุด ตรงกันข้ามกับการสกัดโดยใช้น้ำเพียงอย่างเดียว ความแตกต่างที่เห็นได้ชัดเจนคือผลผลิตของกรดฟีนอลิกและเทอร์พีนอยด์ ซึ่งใน SF70 นั้นสูงกว่าสามเท่าและสูงกว่าเจ็ดเท่าตามลำดับ ผลผลิตการสกัดฟลาโวนอยด์สูงสุดได้มาจากเอทานอล 30% แต่สูงกว่าที่ได้จากเอทานอล 70% เพียงเล็กน้อยเท่านั้น เมื่อพิจารณาจากกลุ่มสารออกฤทธิ์ทางชีวภาพที่ศึกษาทั้งหมด เอทานอล 70% ได้รับการสรุปว่าเป็นตัวทำละลายที่ดีที่สุดในบรรดาสารที่ทดสอบสำหรับการสกัดสารออกฤทธิ์ทางชีวภาพจาก เอส. ฟรุติโคซา.
กิจกรรมต้านอนุมูลอิสระ
การมีอยู่ของสารประกอบที่แสดงฤทธิ์ต้านอนุมูลอิสระในวัสดุจากพืชได้กลายเป็นส่วนสำคัญในการกำหนดคุณสมบัติในการส่งเสริมสุขภาพ ในกรณีของปราชญ์หลากหลายสายพันธุ์ กิจกรรมต้านอนุมูลอิสระสูงมีสาเหตุหลักมาจากสารประกอบฟีนอลิก ในการศึกษาที่นำเสนอ ได้มีการกำหนดฤทธิ์ต้านอนุมูลอิสระทั้งหมด เอส. ฟรุติโคซา สารสกัดที่เตรียมด้วยสารสกัดที่มีขั้วต่างกัน นอกจากนี้ ฤทธิ์ต้านอนุมูลอิสระยังถูกกำหนดไว้สำหรับสารประกอบฟีนอลที่เลือกสรรตามแบบฉบับของเสจและเป็นของสารทุติยภูมิประเภทต่างๆ เช่น กรดฟีนอลิก ฟลาโวน และไดเทอร์พีนอยด์
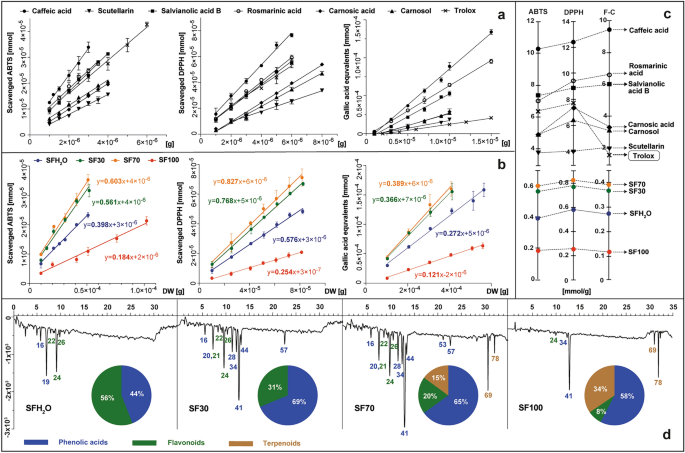
การศึกษาที่นำเสนอเปรียบเทียบผลลัพธ์ของการทดสอบสเปกโตรโฟโตเมตริกที่ได้รับความนิยมสูงสุดสามรายการโดยใช้รีเอเจนต์ ABTS, DPPH และ Folin–Ciocalteu (F–C) การทดสอบ ABTS และ DPPH ถูกนำมาใช้อย่างกว้างขวางเพื่อระบุกิจกรรมการขับอนุมูลอิสระของสารสกัด เช่นเดียวกับสารประกอบบริสุทธิ์ สำหรับ เอส. ฟรุติโคซา สารสกัด ฤทธิ์ต้านอนุมูลอิสระที่คำนวณได้จะอธิบายจำนวนโมเลกุล ABTS หรือ DPPH ที่ลดลงโดยสารต้านอนุมูลอิสระที่ได้มาจากวัสดุแห้ง 1 กรัมหลังจากปฏิกิริยา 10 นาที ค่าเหล่านี้ได้รับการคำนวณในช่วงเชิงเส้นของวิธีการและแสดงเป็นความชันของเส้นที่อธิบายความสัมพันธ์ระหว่างจำนวนมิลลิโมลที่ลดลงของสารออกซิแดนท์และปริมาณต่างๆ ของตัวอย่างที่ทดสอบ – เป็นกรัมของวัตถุแห้งในของผสมปฏิกิริยา (รูปที่. 2ข)
ฤทธิ์ต้านอนุมูลอิสระตามมาตรฐาน (กรดคาเฟอิก, สคูเทลลาริน, กรดซัลเวียโนลิกบี, กรดโรสมารินิก, กรดคาร์โนซิก, คาร์โนซอล และโทรลอกซ์) และ เอส. ฟรุติโคซา สารสกัด : SFH2สารสกัด O-น้ำ; สารสกัดเอทานอล SF30–30%; สารสกัดเอธานอล SF70–70%; สารสกัด SF100–เอธานอล ทดสอบในหลอดทดลองด้วยรีเอเจนต์ ABTS, DPPH และ F–C ที่นำเสนอเป็นแผนที่แสดงเส้นโค้งการพึ่งพาของรีเอเจนต์ที่ลดลงตามมาตรฐานที่ทดสอบ (ก) หรือสารสกัด (ข) และแสดงเป็นความชันของเส้นโค้งเท่ากับไมโลโมลของรีเอเจนต์ลดลง 1 กรัมของตัวอย่างที่ทดสอบ (ค) ตั้งค่าด้วยโปรไฟล์สารต้านอนุมูลอิสระของสารสกัด ซึ่งลงทะเบียนที่ 734 นาโนเมตรหลังการแปลงอนุพันธ์หลังคอลัมน์ด้วย ABTS โดยมีสารต้านอนุมูลอิสระประเภทหลักบนแผนภูมิวงกลม (ง- สำหรับเอกลักษณ์ของยอดเขา ดูตารางเสริม S1.
การศึกษายังรวมถึงวิธีการที่ใช้รีเอเจนต์ Folin–Ciocalteu ประกอบด้วยการถ่ายโอนอิเล็กตรอนในสภาพแวดล้อมที่เป็นด่างจากสารประกอบที่มีกลุ่มไฮดรอกซิลที่ใช้งานอยู่ไปจนถึงคอมเพล็กซ์กรดฟอสโฟโมลิบดิกฟอสโฟทังสติก ความสามารถในการลดในกรณีนี้แสดงเป็นจำนวนมิลลิโมลของกรดแกลลิกที่เทียบเท่ากัน ซึ่งเกิดเป็นสารเชิงซ้อนสีน้ำเงินและได้มาจากวัตถุแห้ง 1 กรัมของพืช วิธีการเดียวกันนี้ใช้กับสารบริสุทธิ์ที่คัดเลือกมาในเสจ เช่น กรดคาเฟอิก กรดคาร์โนซิก คาร์โนซอล กรดซัลเวียโนลิก B สคูเทลลาริน กรดโรสมารินิก และเพิ่มเติมสำหรับสารต้านอนุมูลอิสระอ้างอิง ได้แก่ โทรลอกซ์ (รูปที่. 2ก) วิธีการระบุและคำนวณกิจกรรมต้านอนุมูลอิสระของวัสดุพืชและสารบริสุทธิ์ดังกล่าวได้รับการอธิบายไว้ก่อนหน้านี้โดย Kusznierewicz และคณะ27 และ Baranowska และคณะ28ตามลำดับ ค่าความชันที่ได้จะถูกพล็อตบนแกนที่แยกจากกันสำหรับการทดสอบแต่ละครั้งที่ดำเนินการสำหรับสารมาตรฐานและตัวอย่าง (รูปที่. 2ค). มาตรฐานฟีนอลิกที่ทดสอบแต่ละรายการมีฤทธิ์ต้านอนุมูลอิสระ โดยเพิ่มขึ้นตามลำดับดังนี้: สคิวเทลลาริน < คาร์โนซอล < กรดคาร์โนซิก < กรดซัลเวียโนลิก B < กรดโรสมารินิก < กรดคาเฟอิก กรดซัลเวียโนลิกบี กรดโรสมารินิก และกรดคาเฟอิก มีประสิทธิภาพมากกว่าโทรลอกซ์ ซึ่งเป็นสารประกอบที่ใช้กันทั่วไปเป็นข้อมูลอ้างอิงในการตรวจวัดฤทธิ์ของสารต้านอนุมูลอิสระ ฤทธิ์ต้านอนุมูลอิสระของสารสกัดที่ศึกษาทั้งหมดจาก เอส. ฟรุติโคซา ขึ้นอยู่กับขนาดยาในการทดสอบ ABTS และในการทดสอบ DPPH ดังนั้นเมื่อปริมาณสารสกัดที่เติมลงในส่วนผสมของปฏิกิริยาเพิ่มขึ้น พลังรีดิวซ์ที่มีต่ออนุมูลเหล่านี้ก็จะเพิ่มขึ้นเช่นกัน กิจกรรมต้านอนุมูลอิสระโดยรวมต่ำที่สุดถูกพบสำหรับสารสกัด SF100 ตามมาด้วย SFH ที่สูงขึ้นเกือบสองเท่า2O และสูงกว่าเกือบสี่เท่าสำหรับ SF30 และ SF70 ผลลัพธ์ของการทดสอบ F–C เป็นไปตามแนวโน้มเดียวกันกับ ABTS และ DPPH โดยมีความสัมพันธ์แบบเพียร์สันที่ 0.99 ซึ่งบ่งชี้ว่าฤทธิ์ต้านอนุมูลอิสระของสารสกัดขึ้นอยู่กับปริมาณฟีนอลิกอย่างมาก ดังที่แสดงโดย Lantzouraki และคณะ29.
ขึ้นอยู่กับเนื้อหาของไฟโตเคมิคอลทั้ง 6 ชนิดที่เลือกมาทดสอบในสารสกัด (ตารางที่ 1) 1) และฤทธิ์ต้านอนุมูลอิสระที่กำหนดสำหรับพวกมันและสำหรับสารสกัด (รูปที่. 2a,c) เราสามารถกำหนดการมีส่วนร่วมโดยประมาณของสารประกอบเหล่านี้ต่อฤทธิ์ต้านอนุมูลอิสระทั้งหมดของสารสกัดแต่ละชนิด ในกรณีของ SFH2สารสกัด O, SF30 และ SF70, สารประกอบที่เลือก 6 ชนิด ขึ้นอยู่กับการทดสอบ โดยครอบคลุมในทางทฤษฎี 21–30%, 45–63% และ 64–86% ของฤทธิ์ต้านอนุมูลอิสระทั้งหมดที่กำหนดตามลำดับ ผลลัพธ์เหล่านี้บ่งชี้ว่าอาจมีสารต้านอนุมูลอิสระเพิ่มเติมอื่นๆ ในสารสกัดเหล่านี้ และ/หรือผลเสริมฤทธิ์กันของสารเหล่านี้ เฉพาะในกรณีของสารสกัด SF100 เท่านั้นที่ผลรวมของการออกฤทธิ์ของสารประกอบมาตรฐาน 6 ชนิดเกินกว่าฤทธิ์รวมที่กำหนดของสารสกัดนี้ในช่วงตั้งแต่ 20 ถึง 49% ขึ้นอยู่กับการทดสอบที่ใช้ การสังเกตดังกล่าวอาจเป็นผลมาจากปฏิกิริยาที่เป็นปฏิปักษ์ที่เป็นไปได้ระหว่างสารพฤกษเคมีที่มีอยู่ในสารสกัดประเภทนี้
ข้อมูลรายละเอียดเพิ่มเติมเกี่ยวกับประเภทของสารต้านอนุมูลอิสระที่มีอยู่ในการทดสอบ เอส. ฟรุติโคซา สารสกัดจัดทำโดยการใช้ HPLC หลังคอลัมน์อนุพันธ์กับรีเอเจนต์ ABTS โปรไฟล์ของสารต้านอนุมูลอิสระที่ได้รับจากวิธีนี้ เช่นเดียวกับการมีส่วนร่วมของสารต้านอนุมูลอิสระประเภทต่างๆ ในฤทธิ์ต้านอนุมูลอิสระทั้งหมด จะแสดงไว้ในรูปที่ 1 2ง. นอกจากสารต้านอนุมูลอิสระมาตรฐาน 6 ชนิดที่ทดสอบมาก่อนหน้านี้แล้ว เอส. ฟรุติโคซา สารสกัดยังมีสารต้านอนุมูลอิสระอื่นๆ เช่น przewalskinic acid A, salviaflaside, luteolin rutinoside, luteolin glucoside, isorhamnetin glucuronide, coumaroyl caffeoylglycoside, salvianolic acid K และ salvianolic acid F. ลักษณะโปรไฟล์ที่มีลักษณะเป็นจำนวนและขนาดที่ใหญ่ที่สุดของพีคเชิงลบบ่งชี้ถึงการลดลงและการเปลี่ยนสีของ ตรวจพบอนุมูล ABTS สำหรับสารสกัด SF70 และ SF30 แม้ว่าโปรไฟล์ของสารต้านอนุมูลอิสระของทั้งสองตัวอย่างจะมีความคล้ายคลึงกัน แต่ความเข้มของสัญญาณทั่วไปสำหรับ SF70 ก็สูงกว่าและกิจกรรมเพิ่มเติมที่เกิดจากไดเทอร์พีนอยด์ก็ถูกสังเกตเห็นเช่นกัน เฉพาะในโปรไฟล์ของสารสกัด SF70 และ SF100 เท่านั้นที่มีพีคเชิงลบที่เกิดจากไดเทอร์พีนอยด์ที่สังเกตได้ โดยมีส่วนแบ่งในฤทธิ์ต้านอนุมูลทั้งหมดที่ 15 และ 34% ตามลำดับ สารต้านอนุมูลอิสระหลักในสารสกัดทั้งหมดที่มีเอทานอลคือกรดโรสมารินิก ซึ่งเป็นกรดฟีนอลิกที่มีมากที่สุดและเป็นหนึ่งในสารต้านอนุมูลอิสระที่แข็งแกร่งที่สุดในบรรดามาตรฐานที่ศึกษา มีรายงานผลเช่นเดียวกัน S. officinalis และ เอส. ฮิสปานิกา สารสกัด30,31.
ในสารสกัดที่เป็นน้ำ (SFH2O) ฤทธิ์ต้านอนุมูลอิสระส่วนใหญ่มาจากสารประกอบ 2 ชนิด ได้แก่ กรด przewalskinic A และ scutellarin เนื่องจากการสกัดกรด rosmarinic ด้วยน้ำเพียงอย่างเดียวมีประสิทธิภาพน้อยกว่า
ฤทธิ์ยับยั้งแซนทีนออกซิเดส
เอนไซม์แซนทีนออกซิเดส (XO) เร่งปฏิกิริยาออกซิเดชันของไฮโปแซนทีนและแซนทีนให้เป็นกรดยูริก ซึ่งส่วนเกินในเลือดทำให้เกิดโรคเกาต์ ในระหว่างปฏิกิริยาออกซิเดชันของ XO ออกซิเจนโมเลกุลจะทำหน้าที่เป็นตัวรับอิเล็กตรอน ทำให้เกิดอนุมูลซูเปอร์ออกไซด์และไฮโดรเจนเปอร์ออกไซด์ ด้วยเหตุนี้ XO จึงถือเป็นแหล่งทางชีวภาพที่สำคัญของอนุมูลซูเปอร์ออกไซด์ ซึ่งเมื่อรวมกับออกซิเจนชนิดปฏิกิริยาอื่นๆ มีส่วนทำให้เกิดความเครียดจากปฏิกิริยาออกซิเดชันของร่างกาย และเกี่ยวข้องกับกระบวนการทางพยาธิวิทยาหลายอย่าง เช่น การอักเสบ หลอดเลือด มะเร็ง การแก่ชรา เป็นต้น32- วิธีการรักษาล่าสุดสำหรับการรักษาภาวะกรดยูริกในเลือดสูงคือการยับยั้งเอนไซม์ XO ยาหลายชนิดที่มีสารยับยั้ง XO (allopurinol, febuxostat) ได้รับการพัฒนาขึ้นซึ่งการใช้นั้นน่าเสียดายที่เกี่ยวข้องกับผลข้างเคียงบางอย่าง ด้วยเหตุนี้ จึงมีการค้นหาสารยับยั้ง XO ตามธรรมชาติอย่างต่อเนื่อง ซึ่งสามารถเป็นทางเลือกแทนสารประกอบสังเคราะห์เหล่านี้ได้ มีรายงานบางฉบับในวรรณคดีเกี่ยวกับความสามารถของสัตว์หลายชนิด ซัลเวีย (S. plebeia, S. miltiorrhiza, S. เวอร์บีนาก้า) เพื่อยับยั้ง XO33,34,35ดังนั้นจึงมีการทดสอบเหตุการณ์ที่เป็นไปได้ของกิจกรรมนี้ในการศึกษาด้วย เอส. ฟรุติโคซา สารสกัด นอกจากนี้ ยังมีการพิจารณาฤทธิ์ยับยั้ง XO ในสารประกอบฟีนอลิกที่คัดเลือกมาโดยทั่วไปสำหรับปราชญ์ เช่น กรดคาเฟอิก กรดคาร์โนซิก คาร์โนซอล กรดซัลเวียโนลิก B สคูเทลลาริน กรดโรสมารินิก และนอกจากนี้ อัลโลพิวรินอลซึ่งเป็นตัวยับยั้ง XO ยังเป็นข้อมูลอ้างอิงอีกด้วย
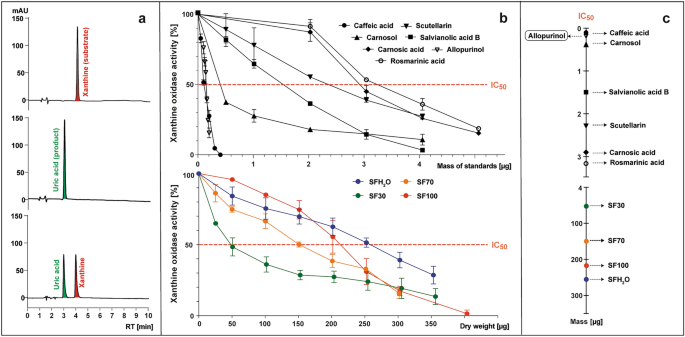
การเปลี่ยนรูปของแซนทีน (สารตั้งต้น) ไปเป็นกรดยูริก (ผลิตภัณฑ์) โดย XO โดยมีหรือไม่มีการมีอยู่ของตัวอย่างที่ทดสอบถูกติดตามด้วยการใช้ HPLC-PAD ที่ 285 นาโนเมตร (รูปที่ 3ก) กิจกรรมของเอนไซม์ถูกคำนวณเป็นเปอร์เซ็นต์ของพื้นที่พีคของกรดยูริกที่เกิดขึ้นต่อหน้าตัวอย่างที่ทดสอบเมื่อเปรียบเทียบกับกลุ่มควบคุมโดยไม่ต้องเติมตัวอย่าง (รูปที่ 3ข) การยับยั้งเอนไซม์ XO แสดงเป็นไอซี50 ค่า ซึ่งหมายถึงมวลของน้ำหนักมาตรฐานหรือน้ำหนักแห้งของตัวอย่าง (ไมโครกรัม) ที่สามารถลดการทำงานของเอนไซม์ลงเหลือ 50% (รูปที่ 3ข,ค)
ตัวอย่างของ HPLC โครมาโตกราฟีที่ 285 นาโนเมตรของของผสมหลังปฏิกิริยาที่มี (จากด้านบน): แซนทีน; แซนทีนและแซนทีนออกซิเดส (XO); แซนทีน XO และสารยับยั้ง (ก) ซึ่งเป็นพื้นฐานในการเตรียมแปลงที่แสดงถึงเส้นโค้งของกิจกรรม XO ต่อหน้ามาตรฐานที่ทดสอบ (กรดคาเฟอีน, สคูเทลลาริน, กรดซัลเวียโนลิกบี, กรดโรสมารินิก, กรดคาร์โนซิก, คาร์โนซอล และอัลโลพิวรินอล) หรือ เอส. ฟรุติโคซา สารสกัด (SFH2สารสกัด O-น้ำ; สารสกัดเอทานอล SF30–30%; สารสกัดเอธานอล SF70–70%; SF100 – สารสกัดเอธานอล) (ข) ซึ่งใช้ในการกำหนดพารามิเตอร์ไอซี50, หมายถึงไมโครกรัมของตัวอย่างที่ทดสอบซึ่งจำเป็นต่อการลดกิจกรรม XO ลงเหลือ 50% (ค).
อัลโลพิวรินอลของตัวยับยั้ง XO ที่เป็นที่รู้จักถูกใช้เป็นข้อมูลอ้างอิง โดยมี IC50 ค่า 0.15 ไมโครกรัม (5.5 µM) มาตรฐานที่ทำการศึกษาทั้งหมดแสดงฤทธิ์ยับยั้ง XO ด้วย IC50 ตั้งแต่ 0.1 ถึง 3.15 ไมโครกรัม (2.8–43.8 µM) กิจกรรมการยับยั้ง XO เพิ่มขึ้นตามลำดับดังนี้ กรด rosmarinic < กรด carnosic < scutellarin < กรด salvianolic B < carnosol < กรดคาเฟอีน กรดคาเฟอิกมีค่า IC ต่ำที่สุด50 ค่า (0.1 ไมโครกรัม; 2.8 ไมโครโมลาร์) ซึ่งบ่งชี้ถึงฤทธิ์ยับยั้ง XO ที่แข็งแกร่งที่สุดในบรรดาสารประกอบที่ทดสอบ มีฤทธิ์แรงกว่าอัลโลพูรินอลเสียอีก ซึ่งไม่สอดคล้องกับข้อมูลที่วรรณและคณะนำเสนอ36 และเฟลมมิก และคณะ37โดยที่ไอซี50 กรดคาเฟอิกต่ำกว่าอัลโลพูรินอลเกือบ 8 หรือ 2 เท่าตามลำดับ ความแตกต่างเหล่านี้อาจเป็นผลมาจากที่มาของ XO ที่เลือกสำหรับการทดสอบ ในการศึกษาที่อ้างถึง มีการใช้ออกซิเดสจากนมวัว ในขณะที่การศึกษานี้เลือกจุลินทรีย์ออกซิเดส ในการศึกษานี้ กรดโรสมารินิกมีฤทธิ์ยับยั้ง XO ต่ำที่สุด (3.2 μg; 43.8 µM) แต่ Ghallab และคณะ38 รายงานว่าการทำงานร่วมกันของ allopurinol และกรด rosmarinic สามารถลดปริมาณยาสังเคราะห์ที่จำเป็นได้ XO ถูกยับยั้งโดยทุกคนที่ศึกษา เอส. ฟรุติโคซา สารสกัดถึงแม้ว่าจะมีประสิทธิภาพน้อยกว่าอัลโลพูรินอลถึง 1,000 เท่าก็ตาม ซึ่งสอดคล้องกับข้อมูลที่รายงานสำหรับสารสกัดอื่นๆ ซัลเวีย สายพันธุ์. Scutellarin และฟลาโวนอื่นๆ ได้รับการอธิบายไว้ก่อนหน้านี้ว่าเป็นสารยับยั้ง XO อย่างแรง39- แม้ว่าปริมาณฟลาโวนอยด์ทั้งหมดจะแตกต่างกันเพียงเล็กน้อยระหว่างสารสกัด SF30 และ SF70 และเนื้อหาของสารประกอบต้านการอักเสบอื่นๆ ที่เป็นประโยชน์ต่อสารสกัด SF70 มากกว่า แต่ SF30 มีความสามารถที่แข็งแกร่งที่สุดในการยับยั้งการทำงานของ XO ไอซี50 ค่าสำหรับ SF30 คือ 50 ไมโครกรัม และตามพารามิเตอร์นี้ ฤทธิ์ต้านการอักเสบที่เป็นไปได้ของ SF70, SF100 และ SFH2สารสกัด O ถูกกำหนดว่าอ่อนกว่า 3, 4 และ 5 เท่าตามลำดับ
[โฆษณา_2]